شیمیایی ریاکسیون
شیمیایی ریاکسیون — کیمیاسال تپکیمه یا رئاکسیون، ایکی ماده یا داها فازلا بیربیری لر اتکیلشمسی. مادهنین ترکیب و خاصهلرینین دیشمسی ایله باش وئرن حادیثهیه کیمیوی حادیثه، شیمیایی ریاکسیون و یا کیمیوی رئاکسیا دئیلیر. کیمیوی رئاکسیالار همیشه فیزیکی حادیثه لرله مۆشایعت اوْلونور. فیزیکی حادیثه زامانی ماده نین ترکیبی دیشمیر، یالنیز فوْرماسی، حجمی و آقرئقات حالی دیشیر. کیمیوی رئاکسیالاری آشاغیداکی خاریجی علامتلره گؤره معیین ائتمک اوْلور:
- ایستیلین آیریلماسی و یا اۇدولماسی
- ایشیغین آیریلماسی
- رنگین دیشمسی
- چؤکونتونون عمله گلمسی و یا ایتمسی
- قاز حالیندا ماده نین آیریلماسی
- آیین چیخماسی.
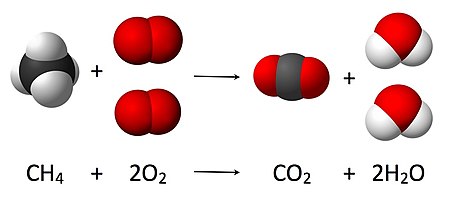
کیمیوی رئاکسیالارین باش وئرمسی اۆچون رئاکسیایا داخیل اوْلان ماده لر بیر-بیری ایله تماسدا اوْلمالی و اکسر حاللاردا قیزدیریلمالیدیر. برک ماده لرین خیردالانماسی و قاریشدیریلماسی رئاکسیانین باشلانماسینا کؤمک ائدیر و رئاکسیانی سۆرتلندیریر. کیمیوی رئاکسیانین گئدیشینین امساللار و فوْرمۇللار واسیطه سیله شرطی یازیلیشینا کیمیوی تنلیک دئیلیر. کیمیوی تنلیکلر ترتیب ائدیلرکن ماده کۆتلسینین ساخلانماسی و ماده ترکیبینین سابیتلی قانۇنلاریندان ایستیفاده ائدیلیر. هر تنلیک اوْخ ایشارسی ایله بیرلشمیش ایکی هیسدن عیبارتدیر. سوْل طرفده رئاکسیایا گیرن ماده لرین، ساغ طرفده ایسه رئاکسیا نتیجسینده آلینان ماده لرین فوْرمۇللاری یازیلیر:2H2 + O2 → 2H2O
رئاکسیادا ایشتیراک ائدن فازالارین ساینا گؤره
دَییشدیرهوْموگئن و هئتئروگئن رئاکسیالار
دَییشدیرهوْموگئن سیستئملرده گئدن کیمیوی رئاکسیالا هوْموگئن رئاکسیا، هئتئروگئن سیستئملرده گئدن کیمیوی رئاکسیالار ایسه هئتئروگئن رئاکسیا آدلانیر.
هوْموگئن رئاکسیالار بیرجینسلی مۆحیطده، ینی قازلار قاریشیغیندا و بیرفازالی مایئ محلوللاردا گئدیر:
H2(q) + F2(q) → 2 HF NaOH(məh) + 2HCl(məh) → NaCl2(məh) + H2O
هئتئروگئن رئاکسیا ایکی و یا داها آرتیق فازانین بؤلگو سطحینده گئدیر. چۆنکی رئاکسیایا داخیل اوْلان ماده لرین موْلئکوللارینین توْققوشماسی یالنیز سطحده مۆمکوندور. بۇنا گؤره هئتئروگئن رئاکسیانین سۆرتینین آرتماسینا سحت بؤیوکلویو، باشقا سؤزل، برک ماده نین خیردالانما (دیرسپئرسلیک) درجسی بؤیوک تأثیر گؤستریر. مثلاً،
CO2(q) + NaOH(məh) → NaHCO3(məh) C(b) + O2(q) → CO2(q)
باشلانغیج ماده لرین و رئاکسیا محصوللارینین سای و ترکیبینه گؤره
دَییشدیربیرلشمه رئاکسیاسی
دَییشدیرایکی و یا داها چوْخ ماده دن بیر مۆرکب ماده نین عمله گلمسی ایله گئدن رئاکسیالارا بیرلشمه رئاکسیالاری دئیلیر.
مۆرکب ماده لر آراسیندا گئدن بیرلشمه رئاکسیالاریندان فرقلی اوْلاراق بسیط ماده لرین بیر-بیری ایله و یا بسیط ماده لرین مۆرکب ماده لرله داخیل اوْلدوغو بیرلشمه رئاکسیالاری اوْکسیدلشم-رئدوکسیا تیپلی اوْلور.
کریستال هیدراتلارین عمله گلمسی ده بیرلشمه رئاکسیالارینا آید ائدیله بیلر:
نئیتراللاشما رئاکسیالاری
دَییشدیراسیدلا تۇرشۇلارین قارشیلیقلی تاثیرینه نئیتراللاشما رئاکسیالاری دئیلیر. نئیتراللاشما رئاکسیاسینین ماهیتی OH¯و H+یوْنلارینین قارشیلیقلی تأثیری نتیجسینده آز دیسوسیاسیا ائدن سۇیون عمله گلمسیندن عیبارتدیر. بۇ ایسه محلۇلون پی اچ-نی ۷-یه یاخینلاشدیریر.
تۇرشو و اسید آراسیندا دوز و سۇیون عمله گلمسیله گئدن رئاکسیالارا نئیتراللاشما رئاکسیالاری دئیلیر.
پارچالانما رئاکسیالاری
دَییشدیربیر مۆرکب ماده دن ایکی و یا داها چوْخ یئنی ماده لرین آلینماسی ایله گئدن رئاکسیالارا پارچالانما رئاکسیالاری دئیلیر.
A → B + C + D
پارچالانما رئاکسیالارینین محصوللاری هم بسیط، هم ده مۆرکب ماده لر اوْلا بیلر.
کریستال هیدراتلارین، اسیدین، بعضی تۇرشۇلارین و بعضی دوزلارین پارچالانماسی رئاکسیالاری ائلئمئنتلرین اوْکسیدلشمه درجلرینین دیشممسی ایله گئدیر:
بیر سیرا پارچالانما رئاکسیالاری ائلئمئنتلرین اوْکسیدلشمه درجلرینین دیشمسی ایله گئدیر. اگر پارچالانما محصوللاریندان هئچ اوْلماسا بیری بسیط ماده دیرس، همین رئاکسیا اوْکسیدلشم-رئدوکسیا مئکانیزمی ایله گئدیر.
کرئکینق، دئهیدروگئنلشمه و دئهیدراتلاشما رئاکسیالاری دا پارچالانما رئاکسیالاریدیر.
عوضئتمه رئاکسیالاری
دَییشدیرمۆرکب ماده نی تشکیل ائدن آتوْملاردان بیرینی و یا بیر نئچسینی دیگر ماده آتوْملارینین عوض ائتمسی ایله گئدن رئاکسیالارا عوضئتمه رئاکسیالاری دئیلیر.
A + BC → AB + C
بسیط و مۆرکب ماده لر آراسیندا گئدن بۆتون عوضئتمه رئاکسیالاری اوْکسیدلشم-رئدوکسیا تیپلیدیر.
2Al + Fe2O3 → 2Fe + Al2O3 Zn + 2HCl → ZnCl2 + H2 2KBr + Cl2 → 2KCl + Br2
بۇ جۆر رئاکسیالاردا داها آکتیو مئتال ائلئکترونلارینی داها آز آکتیو مئتال و یا هیدروگئن آتوْمونا وئریر.
بعضی عوضئتمه رئاکسیالاری اوْکسیدلشمه درجلرینین دیشممسی ایله گئدیر:
بۇ جۆر رئاکسیالار، عادتاً ایکی مۆرکب ماده آراسیندا گئدیر. بئله رئاکسیالارا میثال اوْلاراق سیلیسیۇم-دیوْکسیدله اوْکسیژنلی تۇرشۇلارین دوزلارینین رئاکسیالارینی گؤسترمک اوْلار:
CaCO3 + SiO2 → CaSiO3 + CO2 Ca3(PO4)2 + 3 SiO2 = 3 CaSiO3 + P2O5
دیشمه رئاکسیالاری
دَییشدیرایکی مۆرکب ماده نین ترکیب هیسلرینی دیشرک یئنی ماده لر عمله گتیرمسی ایله گئدن رئاکسیالارا دیشمه (مۆبادیله) رئاکسیالاری دئیلیر.
دیشمه رئاکسیالارینین اکسریتی آتوْملارین اوْکسیدلشمه درجسینین دیشممسی ایله گئدیر.
ZnO + H2SO4 → Zn2SO4 + H2O AgNO3 + NaCl → AgCl + NaNO3 3NaOH + CrCl3 → 3NaCl + Cr(OH)۳
دیشمه رئاکسیالارینین خۆصوصی حالی نئیتراللاشما رئاکسیالاریدیر.
کئچیریلمه (داشینما)
دَییشدیرکئچیریلمه رئاکسیالاریندا آتوْم و یا آتوْم قروپلاری بیر قۇرولۇش واحیدیندن دیگرینه کئچیر.
AB + BC → A + B2C A2B + 2CB2 → ACB2 + ACB3
مثلاً،
2AgCl + SnCl2 → 2Ag + SnCl4
بۇ تیپرئاکسیالار همیشه اوْکسیدلشم-رئدوکسیا کاراکتئرلی اوْلور.
H2O + 2NO2 → HNO3 + HNO2
کئچیریلمه رئاکسیالاری عوضئتمه رئاکسیالارینین معیین فوْرماسی اوْلوب مئکانیزمی ایله اوْندان فرقلنمیر.
رئاگئنتلرین و رئاکسیا محصوللارینین آقرئقات حالینا گؤره
دَییشدیررئاکسیایا داخیل اوْلان و آلینان ماده لرین آقرئقات حالینا گؤره رئاکسیالاری فرقلندیریرلر.<بر/> قازلار آراسیندا گئدن رئاکسیالار:
H2(q) + Cl2(q) → 2HCl(q)
محلۇللار آراسیندا گئدن رئاکسیالار:
NaOH(məh) + HCl(məh) → NaCl(məh) + H2O(m)
برک ماده لر آراسیندا گئدن رئاکسیالار:
CaO(b) + SiO2(b) → CaSiO3(b)